桐树科研 硕果累累丨全外显子测序 细胞实验助力拨开ALK-TKIs早期耐药重重迷雾
首页
ꄲ
桐树科研
ꄲ
桐树科研 硕果累累丨全外显子测序 细胞实验助力拨开ALK-TKIs早期耐药重重迷雾
本文发表于Onco Targets and Therapy
间变性淋巴瘤激酶(ALK)融合基因是非小细胞肺癌(NSCLC)中致癌驱动基因的一个重要部分,约占全球所有病例的3%-7%。小分子酪氨酸激酶抑制剂(TKIs)是ALK基因重排阳性NSCLC患者的标准治疗方法,一代TKI克唑替尼是最常用的靶向药物。然而有研究显示大约20%的ALK重排NSCLC患者在治疗的前6个月对克唑替尼或阿来替尼(二代TKI)产生耐药性,且生存时间不超过12个月,即早期对TKIs产生耐药性的患者预后较差。ALK重排NSCLC患者对一代和二代TKIs的耐药是由多种机制介导的,其中20%-30%的病例发生ALK继发突变,10%的病例发生ALK重排基因扩增。目前尚不清楚ALK融合基因NSCLC患者早期对TKI耐药或预后不良的分子机制。
本研究旨在通过对克唑替尼早期反应较差(PFS≤3个月)与反应良好(PFS≥36个月)的肺腺癌标本进行全外显子测序(WES)和细胞实验以全面了解ALK重排NSCLC对TKI早期耐药的分子机制和预后。
研究涉及87例具有ALK重排并接受克唑替尼治疗的NSCLC患者。为了探讨克唑替尼耐药的分子机制,根据克唑替尼的疗效,选取10例ALK重排NSCLC患者的肿瘤样本进行WES测序。其中5例患者对克唑替尼的反应(中位PFS 2±1个月)显著低于另外5例患者(中位PFS 36±12.8个月)。两组患者在年龄、性别等临床特征上无明显差异。其中有完整随访数据以及样本合格的19例患者用于验证研究(中位PFS和OS分别为15个月和19个月)。
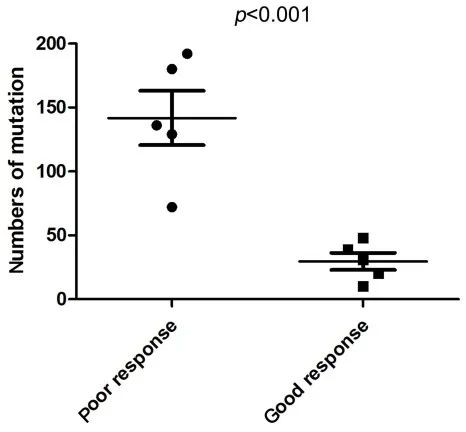
WES测序结果显示10例患者的样本中平均有264个体细胞突变,反应较差组的体细胞突变数较高(P <0.001)。共同突变的中位数在反应良好组为31(10 – 48),而在反应较差组为136(72 – 180),如图1所示。反应较差组的中位TMB高于反应良好组(18 vs 8, P=0.002)。因此,对克唑替尼反应较差的NCLSC患者比反应较好的NCLSC患者有更多的体细胞突变。此外,通路分析的结果与STRING数据库中的功能蛋白分析一致,揭示ALK阳性NSCLC患者的这些遗传变异参与了对克唑替尼治疗或生存的不同反应,而TP53是这些变异的关键因素。
图1. 对克唑替尼反应较差或良好患者组中具有共同基因突变的数量
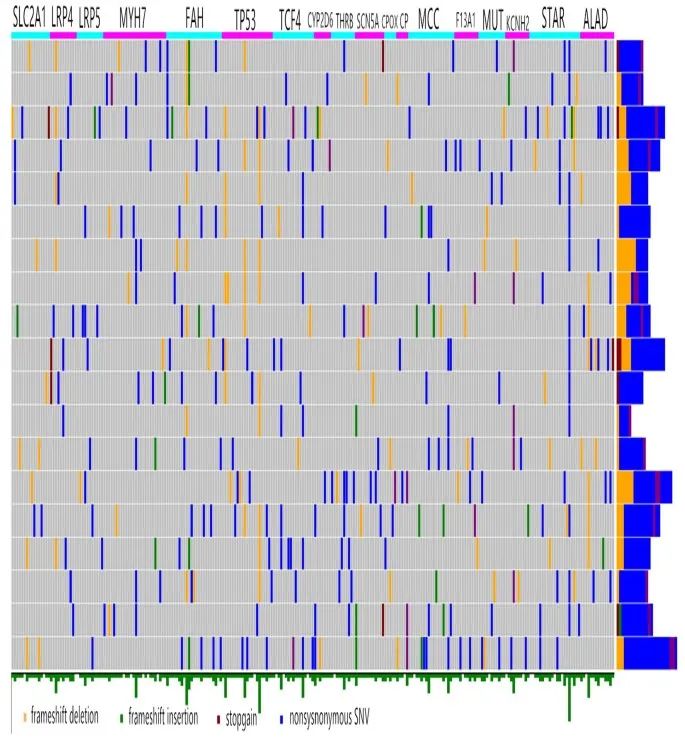
为了验证WES识别的基因突变,本研究选择了43个与肿瘤生长、转移和药物治疗相关的常见突变基因,对19例有ALK重排的NSCLC患者进行基于杂交捕获测序。共有774个基因组变异可以与克唑替尼反应相匹配,它们位于DNA修复、线粒体凋亡和肿瘤血管生成靶基因的区域。这些变异中有20个位于18个基因的编码区,包括SNV、移码缺失和终止突变,如图2所示。其中有TP53外显子3 G245S突变和移码缺失。
图2. NGS是在一个单独合成的面板上进行的,该面板包含了19例验证患者的43个靶基因区域
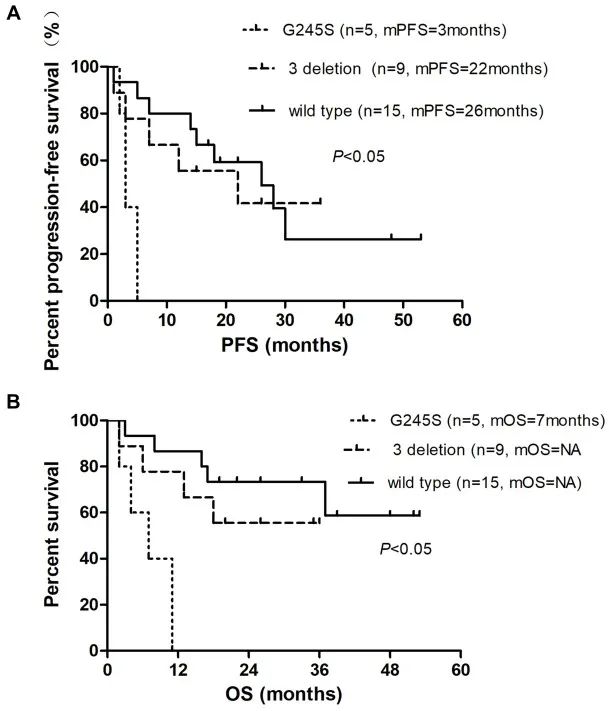
与野生型TP53或外显子3缺失的患者相比,携带TP53 G245S突变的29例患者在克唑替尼治疗后生存时间更短(P<0.05),中位PFS为3个月(95% CI: 1.9-4.1),如图3A所示;中位OS为7个月(95% CI: 3.4-10.5),如图3B所示。这些患者无一存活超过12个月。TP53外显子3缺失组与野生型组PFS或OS无显著性差异。这些结果表明,早期TKI抗性可能是一个包含内在和外在因素的复杂事件。仅TP53 G245S不足以引起TKI抗性。
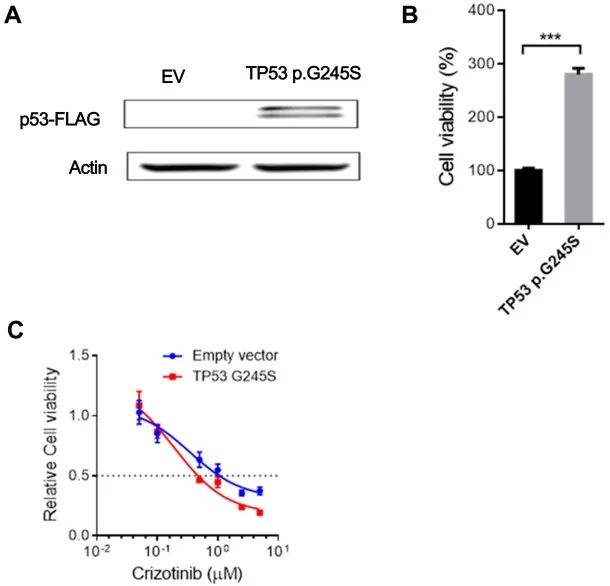
为了确定TP53突变对EML4-ALK重排H3122细胞的影响以及细胞对克唑替尼反应的影响,本研究建立了稳定表达野生型或突变型TP53的细胞,如图4A所示。TP53突变促进H3122细胞增殖约3倍,如图4B所示 (P<0.001)。经过克唑替尼处理后,TP53突变细胞对克唑替尼的敏感性比对照组细胞高,如图4C所示。
图4. 具有TP53 G245S突变的H3122细胞对克唑替尼反应的影响
虽然样本量较小,但本研究表明,高TMB和包括TP53在内的DNA修复基因突变可能主要与ALK重排NSCLC对克唑替尼早期耐药相关,从而导致较差的生存结果。所以需要进一步的前瞻性临床研究来深入证实TP53或DNA修复相关基因变异在ALK-TKI治疗应答或免疫检查点抑制策略对ALK重排NSCLC的作用,有助于为ALK重排NSCLC患者提供更加有效的治疗方法。
文献来源:
Xiao D, Deng Q, He D, et al. High Tumor Mutation Burden and DNA Repair Gene Mutations are Associated with Primary Resistance to Crizotinib in ALK-Rearranged Lung Cancer. Onco Targets Ther. 2021;14:4809-4817. Published 2021 Sep 15.
桐树基因作为一家深耕肿瘤精准医疗领域多年的创新型企业,始终紧跟国际研究前沿,在科研上倾注了大量的精力与资金。
搭建了以肿瘤进化论与肿瘤基因组学标本库为基础的转化性研究中心,从课题设计、研究执行(基因检测)、数据整理及挖掘、文章撰写、投稿修改,提供一站式转化性研究服务。
桐树基因是一家以科技创新为核心、专注于肿瘤精准分子诊断的高科技企业。总部位于上海宝山城工科技绿洲,已分别在上海和常州设立符合GMP标准的生产中心和国际标准的医学临检中心。
桐树基因已经成为国内肿瘤液体活检基因科技的引领者。其全流程ctDNA检测技术,囊括了cfTNA抽提、富集及PRIDE-cfDNA建库技术等核心技术包。基于此推出肿瘤ctDNA检测平台“诊心安”ctDNA核心技术系统化解决方案,其与组织检测一致率高达80%,登顶柳叶刀杂志,比肩国际一流水平。
桐树基因始终坚持“创新•为肿瘤患者创造价值”的宗旨,集肿瘤分子诊断研发、生产、销售一体化,依托“多平台布局”策略,以NGS微量建库技术为核心壁垒的基因检测服务、以肿瘤基因组学标本库为基础的大数据转化研究中心构筑了竞争优势。自主研发的微卫星不稳定检测试剂盒于2021年1月获国内MSI检测首张三类医疗器械注册证,填补了国内精准诊疗领域的空白,造福国内300万肿瘤患者。